
Neurociencia y EducaciÃģn: Âŋpodemos ir de la investigaciÃģn bÃĄsica a su aplicaciÃģn? Un posible marco de referencia desde la investigaciÃģn en dislexia
[Neuroscience and Education: Can we go from basic research to translation? A possible framework from dyslexia research]
Usha Goswami1
1Univ. Cambridge, Centre for Neuroscience in Education, Reino Unido
https://doi.org/10.1016/j.pse.2015.08.002
Resumen
La neurociencia podría transformar la educación, pues proporciona nuevos métodos para comprender el aprendizaje y el desarrollo cognitivo, sus mecanismos causales y una forma empírica de evaluar la eficacia de diferentes pedagogías. No obstante, éste sería un objetivo a largo plazo. Desde la neurociencia educativa se debería empezar estudiando cómo los sistemas cognitivos se construyen sobre los sensoriales a lo largo del desarrollo. Aquí me centraré en el lenguaje. Pequeñas diferencias individuales iniciales en una función sensorial, por ejemplo la auditiva, podrían ser el origen de notables diferencias individuales en el desarrollo lingüístico. La neurociencia podría proporcionar una comprensión detallada de los mecanismos causales del desarrollo que vinculan la audición, el desarrollo fonológico y el desarrollo de la alfabetización. Este tipo de investigación neurocientífica básica podría orientar al campo de la educación y la pedagogía explorando los efectos que sobre estos mecanismos ejercen diferentes contextos pedagógicos y de aprendizaje.
Abstract
Neuroscience has the potential to transform education because it provides novel methods for understanding human learning and cognitive development. It therefore offers deeper understanding of causal mechanisms in learning and an empirical approach to evaluating the efficacy of different pedagogies. However, this will be a long-term enterprise and there will be few immediate pay-offs. Here I set out one possible framework for linking basic research in neuroscience to pedagogical questions in education. I suggest that the developing field of educational neuroscience must first study how sensory systems build cognitive systems over developmental time. I focus on one cognitive system, language, the efficient functioning of which is critical for reading acquisition. Small initial differences in sensory function, for example auditory function, have the potential to cause large differences in linguistic performance over the learning trajectory. The tools offered by neuroscience can enable better understanding of the causal developmental mechanisms linking audition, phonological development and literacy development, in fine-grained detail. Following this basic research, neuroscience can then inform education and pedagogy by exploring the effects on these neural mechanisms of different learning contexts and pedagogies.
En la medicina y en los tratamientos mÃĐdicos se han producido no avances a medida que se ha ido mejorando la comprensiÃģn de la fisiologÃa corporal. Es probable que se produzcan no avances en la educaciÃģn y la eficacia pedagÃģgica a medida que vayamos comprendiendo mejor la fisiologÃa del aprendizaje, que estÃĄ siendo estudiada por neurocientÃficos, quienes estÃĄn descubriendo unos mecanismos que se asemejan a las âleyes generales del aprendizajeâ propuestas hace tiempo desde la psicologÃa. En educaciÃģn, sin embargo, es normal cuestionar la validez del propio concepto de leyes generales del aprendizaje, sobre la base de que el aprendizaje y las capacidades de los individuos estÃĄn inextricablemente unidos a contextos y situaciones de aprendizaje ( Wells y Claxton, 2002 ). Sin embargo, cuando entendamos cÃģmo ocurre el aprendizaje en el cerebro para los diferentes dominios de relevancia educativa, podremos estudiar los efectos de diferentes contextos y situaciones sobre el aprendizaje dentro de un dominio particular. Podemos evaluar directamente los efectos de diferentes ÃĄmbitos de aprendizaje sobre la fisiologÃa del cerebro. En principio, esta aproximaciÃģn permite el desarrollo de una base empÃrica para la educaciÃģn, investigando los efectos de diferentes pedagogÃas y su impacto sobre el aprendizaje en diferentes contextos y situaciones. Sin duda, si la educaciÃģn quisiera adherirse a las promesas de la neurociencia, serÃa posible estudiar cuestiones educativas clave usando aproximaciones cientÃficas y neurocientÃficas tradicionales.
Hasta la fecha ha existido un gran escepticismo entre algunos investigadores del ÃĄmbito educativo sobre el valor de esta perspectiva en su totalidad. Algunos han argumentado que acercarse a la educaciÃģn a travÃĐs del examen empÃrico de la fisiologÃa cerebral confunde âcuestiones que tienen que ver con la naturaleza del conocimiento y cÃģmo aprendemos, lo que constituye un ser humano y su buen hacerâ ( Cigman y Davis, 2009 , p. ix). AsÃ, los mÃĐtodos âreduccionistasâ de la neurociencia se consideran una metodologÃa inadecuada para mejorar nuestro conocimiento de la esencia humana. âÂŋExactamente, en quÃĐ se sustenta la autoridad de la neurociencia para hacer afirmaciones sobre la naturaleza del aprendizaje?â ( Cigman y Davis, 2009, p. 76).
En este artÃculo, elaborado a partir de una conferencia inaugural en el Centre for Educational Neuroscience de Londres, intentarÃĐ mostrar a travÃĐs del ejemplo ilustrativo de la investigaciÃģn en lectura/dislexia que la neurociencia tiene âautoridadâ para realizar descubrimientos fisiolÃģgicos susceptibles de comprobaciÃģn empÃrica y falsaciÃģn. Espero demostrar que el uso de estos mÃĐtodos âreduccionistasâ puede enriquecer considerablemente nuestra comprensiÃģn del aprendizaje en niÃąos y cÃģmo desarrollar su potencial de la mejor manera posible. ComenzarÃĐ revisando brevemente lo que sabemos acerca de la lectura y su desarrollo desde la investigaciÃģn educativa y psicolÃģgica. A continuaciÃģn me centrarÃĐ en los procesos sensoriales bÃĄsicos que probablemente subyazcan a algunos de los factores clave del desarrollo identificados por este tipo de investigaciones. DescribirÃĐ los modelos de procesamiento sensorial bÃĄsico que considero relevantes para comprender el desarrollo del lenguaje y mostrarÃĐ cÃģmo pueden aplicarse sistemÃĄticamente estos modelos al estudio de factores causales del desarrollo y por tanto para proponer pedagogÃas efectivas en la enseÃąanza de la lectura.
Mi objetivo general es proporcionar un esquema verosÃmil de cÃģmo puede utilizarse la neurociencia educativa para ayudar en la prÃĄctica educativa. Este esquema se basa en una serie de principios que he encontrado Útiles en mi propia investigaciÃģn. En primer lugar, deberÃamos preguntarnos quÃĐ sabemos a partir de la investigaciÃģn comportamental disponible sobre un determinado aspecto educativo, como por ejemplo la lectura, el cÃĄlculo, la atenciÃģn o la motivaciÃģn de logro. En segundo lugar, como la neurociencia es ideal para el estudio de procesos sensoriales bÃĄsicos, deberÃamos preguntarnos quÃĐ procesos sensoriales son probablemente importantes a la hora de explicar las diferencias individuales. En tercer lugar, deberÃamos ver si la investigaciÃģn actual en neurociencia nos ofrece modelos teÃģricos relevantes sobre el desarrollo y, a continuaciÃģn, deberÃamos comprobar si estos modelos propician predicciones contras sobre las funciones sensoriales y cognitivas a lo largo del desarrollo. Por Último, necesitamos decidir cÃģmo poner a prueba estas predicciones mediante las tÃĐcnicas de neuroimagen en niÃąos. En el campo de la lectura y la dislexia, mi conclusiÃģn serÃĄ que la neurociencia ofrece ideas y mÃĐtodos muy relevantes para poner a prueba la eficacia de aproximaciones pedagÃģgicas educativas centradas en la importancia del lenguaje oral. Algunos autores sugieren que el juego lingÞÃstico, la poesÃa, las nanas, las canciones infantiles e incluso el entrenamiento musical son de suma importancia para labrar la imaginaciÃģn de los niÃąos ( Styles, Joy y Whitley, 2010 ). Aquà argumentarÃĐ que, gracias a los estudios neurocientÃficos con biofeedback , ahora disponemos de medios tecnolÃģgicos con los que podemos medir tambiÃĐn si estas aproximaciones afectan a los mecanismos neuronales relevantes en el desarrollo del lenguaje y de la alfabetizaciÃģn.
ÂŋQuÃĐ sabemos actualmente?La adquisiciÃģn de la lectura en niÃąos viene determinada, en todos los idiomas, por diferencias individuales en la toma de conciencia por parte de los niÃąos de las estructuras fonolÃģgicas (basadas en el sonido) del lenguaje ( Ziegler y Goswami, 2005 ). La investigaciÃģn psicolÃģgica y educativa ha demostrado esto pidiendo a niÃąos pre-lectores y lectores que completen tareas orales simples tales como contar el nÚmero de sÃlabas de las palabras (2 sÃlabas en âganchoâ, 3 sÃlabas en âradioâ), decidiendo si dos palabras riman (âgato-patoâ, sÃ, âgato-gotaâ, no ) y si empiezan con el mismo sonido (âmarâ âmuroâ â sà ). La ejecuciÃģn en estas tareas es predictiva de la capacidad lectora tanto en lenguajes alfabÃĐticos, como el inglÃĐs o el alemÃĄn (p. ej., Frith, Wimmer y Landerl, 1998 ), como en lenguajes no alfabÃĐticos como el chino (p. ej., Siok y Fletcher, 2001 ). MÃĄs recientemente, se ha demostrado que la conciencia fonolÃģgica âsuprasegmentalâ tambiÃĐn es importante a la hora de explicar diferencias individuales en la lectura ( Goswami, Gerson y Astruc, 2010; Whalley y Hansen, 2006; Wood y Terrell, 1998 ). La conciencia suprasegmental se refiere a la conciencia de los patrones prosÃģdicos y de entonaciÃģn que caracterizan al habla conectada cuando la unidad de anÃĄlisis fonolÃģgico es la oraciÃģn o frase completa y no la palabra. De hecho, existen investigaciones que sugieren que a medida que se desarrolla un lÃĐxico de formas de palabra habladas, tanto la informaciÃģn fonÃĐtica (âsegmentalâ) como la prosÃģdica (âsuprasegmentalâ) estÃĄn inextricablemente unidas entre sà en cuanto a la informaciÃģn fonolÃģgica almacenada por el cerebro para cada forma de palabra (p. ej., Pierrehumbert, 2003).
La estructura fonolÃģgica diferirÃĄ entre lenguas, obviamente, de manera que los predictores fonolÃģgicos de una alfabetizaciÃģn eficiente tambiÃĐn serÃĄn diferentes. Por ejemplo, el chino es un lenguaje tonal. SÃlabas idÃĐnticas poseen significados diferentes cuando se expresan con entonaciones diferentes (p. ej., subir el tono a lo largo de la sÃlaba vs. mantener el tono a lo largo de la sÃlaba). Para lenguajes como el chino, como cabrÃa esperar, la conciencia del tono es tambiÃĐn un predictor importante de la adquisiciÃģn de la alfabetizaciÃģn (p. ej., McBride-Chang, Shu, Zhou, Wat, & Wagner, 2003 ). Al igual que ocurre con las habilidades fonolÃģgicas, las diferencias individuales en otros aspectos de la conciencia lingÞÃstica tambiÃĐn pueden ser importantes para la alfabetizaciÃģn. Un ejemplo es la conciencia morfolÃģgica, donde los niÃąos tienen que prestar atenciÃģn a los significados de las palabras (p. ej., ÂŋcÃģmo se llama el ÃĄrbol en el que crecen los zapatos? - La horma) [en el original en inglÃĐs se juega con el doble significado de la palabra âtreeâ, que significa ÃĄrbol y horma de zapato: âWhat is a tree that grows shoes called? A shoe treeâ]. Como se puede ver, todas estas habilidades que son predictivas de la alfabetizaciÃģn estÃĄn basadas en tareas de procesamiento lingÞÃstico oral. El input para el anÃĄlisis del niÃąo es un patrÃģn sonoro o un grupo de patrones sonoros. Actualmente se cree que la unidad perceptiva esencial que refleja estas estructuras en todas las lenguas es la sÃlaba y no el fonema (p. ej., Greenberg, 2006; Port, 2007).
Asimismo, estas diferentes habilidades fonolÃģgicas y de otro tipo se muestran mermadas en niÃąos con dislexia del desarrollo. El mejor predictor en todas las lenguas de quiÃĐn tendrÃĄ problemas para adquirir la ortografÃa de su idioma es la conciencia fonolÃģgica ( Ziegler y Goswami, 2005; Ziegler et al., 2010 ). Este es el caso independientemente de que el sistema ortogrÃĄfico sea alfabÃĐtico y trabaje en el âgrano finoâ del fonema o de que use caracteres que puedan corresponder a âgranos mÃĄs gruesosâ tales como las sÃlabas (como en el kana japonÃĐs) o incluso palabras enteras (como en el kanji chino). Los niÃąos con dislexia en lenguas tan diversas fonolÃģgica y ortogrÃĄficamente como el inglÃĐs, el italiano y el chino muestran todos ellos dificultades fonolÃģgicas ( Ziegler y Goswami, 2005 , para una visiÃģn general). A pesar de las diferencias fonolÃģgicas y ortogrÃĄficas que existen entre las distintas lenguas, los trabajos actuales en neurociencia cognitiva sugieren que los sistemas neuronales esenciales que se activan tanto durante el procesamiento del lenguaje como durante el procesamiento ortogrÃĄfico (lectura) son muy similares en todas las lenguas (vÃĐase Price y McCrory, 2005 , para una discusiÃģn general). Las redes neuronales que se activan durante tareas de lenguaje y de lectura en diferentes lenguajes son en gran medida las mismas estructuras fisiolÃģgicas. Por tanto, si queremos comprender los procesos sensoriales que subyacen al desarrollo del sistema cognitivo que se emplea en ser lector, que es el lenguaje hablado, una forma de hacerlo es estudiar cÃģmo codifica el cerebro las entradas sonoras, tanto lingÞÃsticas como no lingÞÃsticas. Esta perspectiva asume que la alfabetizaciÃģn es dependiente de la eficacia en el procesamiento del lenguaje oral y no supone la existencia de procesos neuronales adicionales (p. ej., Krafnick, Flowers, Napoliello y Eden, 2011 ). Aquà no tendrÃĐ en cuenta el procesamiento visual, que lÃģgicamente es tambiÃĐn importante para el aprendizaje de la lectura ( Blomert, 2011 ), si bien las habilidades visuales no parecen relacionarse de forma sistemÃĄtica con las diferencias individuales en la capacidad lectora ( Vellutino, Fletcher, Snowling y Scanlon, 2004 ).
ÂŋQuÃĐ procesos sensoriales es probable que sean importantes?El sentido primario que subyace a la percepciÃģn del habla es el auditivo. Investigaciones recientes han mostrado que los bebÃĐs escuchan hablar incluso estando en el Útero, si bien lo que mejor escuchan son las modulaciones de baja frecuencia del habla. Escuchar modulaciones de baja frecuencia es similar a escuchar a alguien hablando bajo el agua âla estructura silÃĄbica bÃĄsica de su habla se puede percibir, pero no siempre las palabras exactas. Estas investigaciones sugieren que los bebÃĐs nacen con algÚn tipo de conciencia de los patrones rÃtmicos caracterÃsticos de su lengua nativa, el lenguaje que ya han escuchado cuando su madre hablaba, y de hecho los neonatos pueden distinguir su lengua nativa de otras lenguas, asà como lenguas con clases diferentes de ritmos. Por ejemplo, los niÃąos de 4 dÃas son sensibles a las diferencias en ritmo y prosodia que caracterizan al holandÃĐs frente al japonÃĐs ( Mehler et al., 1988 ). Una vez que el bebÃĐ interactÚa con sus interlocutores sociales, sin embargo, las claves proporcionadas por la informaciÃģn visual de los labios, la mandÃbula y las mejillas complementan la informaciÃģn auditiva por otras vÃas importantes (p. ej., Kuhl, 2004 ). Estas habilidades de âlectura del hablaâ son importantes para un procesamiento eficiente del lenguaje oral, no solo para individuos sordos, que no tienen acceso a ningÚn tipo de informaciÃģn auditiva. Esto se puede comprobar fÃĄcilmente en el âefecto cocktailâ, por el que resulta mÃĄs fÃĄcil seguir una conversaciÃģn en un ambiente ruidoso cuando puedes ver la boca del hablante mientras escuchas lo que dice. Resulta interesante que la neurociencia de la audiciÃģn muestre que un aspecto fundamental de la informaciÃģn visual con respecto a la inteligibilidad del habla es la informaciÃģn visoespacial de baja frecuencia de los movimientos de apertura y cierre de la mandÃbula. Cuando abrimos y cerramos las mandÃbulas para producir sÃlabas, se genera una informaciÃģn visual dinÃĄmica de baja frecuencia centrada en torno a 4 Hz ( Chandrasekaran, Trubanova, Stillittano, Caplier y Ghazanfar, 2009 ). La informaciÃģn auditiva de baja frecuencia en el habla se corresponde con la estructura silÃĄbica y ronda los 4-6 Hz (Drullman, 2006 ). Por lo tanto, aquà convergen mecanismos fisiolÃģgicos auditivos y visuales para aumentar la eficacia en el procesamiento del lenguaje, tanto en tÃĐrminos perceptivos como motores, pues los bebÃĐs aprenden a producir un lenguaje hablado que pueda ser interpretado por sus interlocutores sociales.
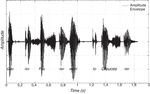
La investigaciÃģn sobre las diferencias individuales en las habilidades de procesamiento auditivo bÃĄsico sugiere que algunos procesos auditivos bÃĄsicos estÃĄn alterados en niÃąos con dislexia del desarrollo ( Goswami, 2009 , para una visiÃģn general). En lugar de revisar todo el campo (vÃĐase HÃĪmÃĪlÃĪinen, Salminen y LeppÃĪnen, 2013 , para una revisiÃģn reciente), aquà me centrarÃĐ en nuestra propia investigaciÃģn, que aporta datos neurocientÃficos relevantes respecto al encadenamiento silÃĄbico del flujo del habla y a la percepciÃģn de la informaciÃģn de baja frecuencia, que discutirÃĐ en detalle posteriormente. A lo largo de la pasada dÃĐcada hemos llevado a cabo una serie de estudios que sugieren que las dificultades auditivas primarias de los niÃąos con problemas de lectura o del habla implican al procesamiento de la envolvente de amplitud ( Corriveau y Goswami, 2009; Corriveau, Pasquini y Goswami, 2007; Goswami, 2009; Goswami et al., 2010; Goswami et al., 2002; Goswami, Wang et al., 2011; Muneaux, Ziegler, Truc, Thomson y Goswami, 2004; Pasquini, Corriveau y Goswami, 2007; Thomson, Fryer, Maltby y Goswami, 2006; Thomson y Goswami, 2008; Richardson, Thomson, Scott y Goswami, 2004 ). La envolvente de amplitud del habla se refiere a las fluctuaciones en la intensidad del sonido que llegan a los tÃmpanos cuando escuchamos el lenguaje hablado (vÃĐase la fig. 1 ). A medida que se produce el habla, la energÃa (o amplitud, cantidad de sonido generada por el hablante) aumenta y disminuye a medida que se producen las sÃlabas y las mandÃbulas se abren y cierran. El oÃdo detecta las diferentes bandas de frecuencia del habla contenidas en el perfil de amplitud y usa tanto la informaciÃģn de amplitud (intensidad sonora) como la de frecuencia para codificar la seÃąal. Neuronalmente, el sistema auditivo codifica la modulaciÃģn de la amplitud en sonidos naturales tanto a lo largo de diferentes bandas de frecuencia como a diferentes escalas temporales ( Joris, Schreiner y Rees, 2004 ). Cuando se produce una sÃlaba, la energÃa aumentarÃĄ cuando se abre la boca, mostrando su mayor valor en el momento de producciÃģn de la vocal, de ahà que las sÃlabas puedan ser descritas como âarcos de energÃaâ ( Greenberg, 2006 ). El tiempo de subida hasta la vocal, es decir, del comienzo de la envolvente de amplitud asociada con una sÃlaba particular, es un elemento crucial de la seÃąal hablada que facilita la segmentaciÃģn temporal de dicha seÃąal en sÃlabas. El tiempo de subida tambiÃĐn se relaciona con las caracterÃsticas de la sÃlaba: el tiempo de subida serÃĄ rÃĄpido si la sÃlaba comienza con un sonido implosivo, como BA, y lento si la sÃlaba comienza con un sonido mÃĄs sonoro, como WA ( Goswami, Fosker, Huss, Mead, & SzÞcs, 2011 ). Conductualmente, el tiempo de subida tambiÃĐn se relaciona con el tiempo del ritmo, tanto en el lenguaje como en la mÚsica, en todas las lenguas, sean del tipo de ritmo que sean, tanto en la percepciÃģn como en la producciÃģn ( Gordon, 1987; Hoequist, 1983; Morton, Marcus y Frankish, 1976; Scott, 1998a ). En nuestros estudios hemos evaluado el procesamiento del tiempo de subida, de la duraciÃģn, la intensidad y la frecuencia de tonos no lingÞÃsticos en niÃąos con un desarrollo tÃpico y lo hemos comparado con los resultados obtenidos en niÃąos con dislexia del desarrollo o con trastorno especÃfico del lenguaje (TEL). Nuestros datos muestran que las dificultades en el procesamiento fonolÃģgico que encontramos en ambos trastornos del desarrollo estÃĄn Ãntimamente relacionadas con un deficiente procesamiento auditivo bÃĄsico del tiempo de subida.
Muestra esquemÃĄtica de la forma de la onda correspondiente a la primera oraciÃģn de la canciÃģn infantil tradicional inglesa âDoctor Foster went to Gloucesterâ, con la envolvente de amplitud (amplitud envolvente) marcada en gris, mostrando que las sÃlabas acentuadas (âDocâ, âFosâ, âwentâ y âGlosâ) tienden a producirse con mayor intensidad que las sÃlabas no acentuadas.
La existencia de dificultades en la percepciÃģn del tiempo de subida sugiere la presencia de dificultades para distinguir los diferentes rangos de modulaciÃģn de las frecuencias del habla ( Goswami, 2011 ). En nuestros estudios, las diferencias individuales en la severidad de las deficiencias en el tiempo de subida son altamente predictivas del grado de deficiencia fonolÃģgica que encontramos en los diferentes niÃąos. Hemos interpretado estos resultados como prueba de que la percepciÃģn del tiempo de subida es crucial para el desarrollo de las representaciones fonolÃģgicas de alta calidad del lenguaje, necesarias para la adquisiciÃģn de la alfabetizaciÃģn. HistÃģricamente, el tiempo de subida se habÃa asociado con la experiencia perceptiva del ritmo y la entonaciÃģn del lenguaje. El tiempo de subida es fundamental para la percepciÃģn de la prosodia ( Greenberg, 2006 ), aunque no sea mencionado en las teorÃas clÃĄsicas de la percepciÃģn prosÃģdica (que asumen que los cambios en la frecuencia fundamental, la duraciÃģn y la amplitud gobiernan la percepciÃģn de la prosodia, teniendo la frecuencia fundamental el papel protagonista, p. ej., Fry, 1954 ). La discriminaciÃģn del tiempo de subida es deficiente en niÃąos con dislexia que hablan inglÃĐs, francÃĐs, hÚngaro, espaÃąol, chino y finÃĐs ( Goswami et al., 2002; Goswami, Wang et al., 2011; HÃĪmÃĪlÃĪinen et al., 2009; Muneaux et al., 2004; Richardson, Thombon, Scott y Goswami, 2004; SurÃĄnyi et al., 2009 ). El tiempo de subida es un predictor significativo de la conciencia fonolÃģgica correspondiente a estos lenguajes (p. ej., conciencia del ritmo en inglÃĐs, vs. conciencia del tono lÃĐxico [subida o bajada del tono de la sÃlaba] en chino). TambiÃĐn estÃĄ muy asociado con la conciencia prosÃģdica y rÃtmica, como se discutirÃĄ posteriormente.
ÂŋExiste un buen modelo neurocientÃfico del desarrollo?La neurociencia de la audiciÃģn ofrece una serie de modelos que permiten comprender cÃģmo se puede representar y codificar la informaciÃģn sensorial auditiva en las ÃĄreas del cerebro que estÃĄn activas durante el procesamiento lingÞÃstico. DiscutirÃĐ uno de estos modelos en profundidad, pues en mi opiniÃģn es sumamente relevante para comprender los vÃnculos causales existentes entre el procesamiento sensorial auditivo bÃĄsico, el desarrollo de la conciencia fonolÃģgica y las habilidades lingÞÃsticas orales, y por tanto la adquisiciÃģn de la lectura y la dislexia. Se trata del modelo del procesamiento de lenguaje de resoluciÃģn multi-temporal de Hickok y Poeppel (2007; vÃĐase tambiÃĐn Poeppel, Idsardi y van Wassenhove, 2008 ). SegÚn dicho modelo, basado en sus propias investigaciones asà como en multitud de otros datos, en la organizaciÃģn cortical del procesamiento del habla intervienen dos sistemas, el ventral y el dorsal. El sistema ventral procesa las seÃąales lingÞÃsticas para la comprensiÃģn, mientras que el dorsal vincula las seÃąales acÚsticas del habla con redes articulatorias del lÃģbulo frontal. El habla es una seÃąal que el cerebro procesa a lo largo del tiempo y es una seÃąal temporalmente compleja. Muchas frecuencias varÃan a diferentes escalas temporales y a diferentes intensidades. Hickok y Poeppel por tanto proponen que la corteza procesa el habla en mÚltiples escalas temporales simultÃĄneamente. Se cree que esto se consigue a partir de las oscilaciones neurales, que discutiremos mÃĄs adelante. Por ahora, lo que quiero destacar es que su modelo postula dos tasas temporales clave, una âsuprasegmentalâ o silÃĄbica (con una ventana larga de integraciÃģn temporal de entre 150 y 300 ms) y una tasa âsegmentalâ o âfonÃĐmicaâ (sonido lingÞÃstico), con una ventana de integraciÃģn temporal corta de en torno a 20-50 ms. En su modelo, la escala temporal larga conlleva claves respecto a los lÃmites silÃĄbicos y la tasa de sÃlabas. TambiÃĐn contiene informaciÃģn tonal, claves prosÃģdicas y claves de acentuaciÃģn. La tasa temporal mÃĄs corta se necesita para determinar el orden de los segmentos sonoros del habla (p. ej., en la palabra âpotrilloâ frente a âportilloâ). La escala temporal mÃĄs corta tambiÃĐn se relaciona con las caracterÃsticas que varÃan cuando producimos diferentes sonidos, tales como el tiempo de inicio de la sonoridad [en inglÃĐs, âvoice onset timeâ] (la diferencia en el inicio de la vibraciÃģn de las cuerdas vocales cuando producimos/b/vs./p/, que varÃa en torno a 40 ms). De esta manera, durante el desarrollo, ambas escalas temporales estÃĄn Ãntimamente relacionadas no solo con la percepciÃģn del habla (p. ej., de sÃlabas vs. fonemas), sino tambiÃĐn con la producciÃģn del habla (p. ej., de sÃlabas vs. variables fonÃĐticas).
Se piensa que las diferentes escalas temporales se âunificanâ cuando se percibe el habla, posibilitando que las entradas de otras modalidades sensoriales tambiÃĐn contribuyan a la percepciÃģn del habla (p. ej., las claves visuales procedentes de los movimientos de labios y mejillas ya comentadas). AdviÃĐrtase que âunificarâ es un concepto utilizado de muy diferentes maneras dentro de la neurociencia y que Hickok y Poeppel (2007) se refieren a algo distinto de lo que expone Blomert (2011) cuando discute sobre la unificaciÃģn. Pensando en este modelo en relaciÃģn al desarrollo fonolÃģgico de los niÃąos, parece evidente que al menos 3 tipos de informaciÃģn sensorial deberÃan ser importantes durante el desarrollo. Se trata de la integraciÃģn temporal de la sÃlaba a escalas temporales mÃĄs largas, la integraciÃģn temporal del fonema a escalas temporales mÃĄs cortas y la integraciÃģn intermodal audiovisual (AV) o unificaciÃģn AV. Por tanto, cabe esperar que una ineficacia neural en el procesamiento de uno cualquiera de estos aspectos de la informaciÃģn sensorial afecte al curso del desarrollo durante el desarrollo fonolÃģgico. De nuevo, necesitamos tener en cuenta lo que ya sabemos. De hecho, estudios realizados con niÃąos muestran que los bebÃĐs con un desarrollo tÃpico procesan ambas escalas temporales del habla desde el nacimiento. Como ya hemos seÃąalado, los niÃąos reciÃĐn nacidos pueden distinguir lenguas en funciÃģn de sus propiedades silÃĄbicas o rÃtmicas y los niÃąos evaluados en el primer mes de vida tambiÃĐn pueden discriminar diferencias fonÃĐticas en la informaciÃģn contenida en ventanas temporales cortas, por ejemplo la discriminaciÃģn entre âbaâ y âpaâ ( Eimas, Siqueland, Jusczyk y Vigorito, 1971 ). Finalmente, los niÃąos pequeÃąos estÃĄn muy capacitados para detectar contrastes auditivo-visuales en el habla, por ejemplo enfadÃĄndose y llorando si se les hacer ver un video de una cabeza hablando desincronizadamente con respecto a lo que estÃĄn oyendo ( Dodd, 1979).
ÂŋCÃģmo codifica el cerebro la informaciÃģn a estas diferentes escalas? Una serie de estudios recientes en animales utilizando registros electrofisiolÃģgicos unicelulares en las cortezas sensoriales primarias y multisensoriales muestran que el cerebro utiliza procesos oscilatorios a diferentes escalas temporales para maximizar la fuerza de representaciÃģn de la informaciÃģn. En humanos y en relaciÃģn al habla, parece probable que las oscilaciones neuroelÃĐctricas en las diferentes bandas de frecuencia segmentan eficazmente el habla entrante en âpaquetesâ de informaciÃģn de diferentes âgranosâ. Estos paquetes de informaciÃģn, tales como la sÃlaba vs. la variable fonÃĐtica, se pueden contrastar con representaciones almacenadas y asà ser interpretados. A travÃĐs de la sincronizaciÃģn de fase (acoplamiento rÃtmico) a las frecuencias entrantes, el cerebro puede seguir la dinÃĄmica del habla por encima de la variabilidad entre hablantes (la tasa de habla variarÃĄ en funciÃģn del hablante, pero los paquetes de informaciÃģn proporcionados por cada hablante estarÃĄn organizados en base a las distintas escalas temporales dentro de la envolvente de amplitud del habla de un individuo, p. ej., sÃlabas, variables fonÃĐticas, etc.). De esta manera, la corteza auditiva analiza y discrimina las oraciones habladas, permitiendo asà la comprensiÃģn del habla.
Los datos en animales sugieren que los diferentes ritmos oscilatorios remiten a diferentes âlaboresâ de integraciÃģn de la seÃąal sensorial (p. ej., Kayser, Petkov y Logothetis, 2008; Lakatos, Chen, OâConnell, Mills y Schroeder, 2007 ). Por ejemplo, las oscilaciones de baja frecuencia gobiernan las influencias de la corteza auaditiva sobre el ÃĄrea multimodal para la unificaciÃģn auditivo-visual, el surco temporal superior (STS). Las oscilaciones de mÃĄs alta frecuencia gobiernan las influencias del STS sobre la corteza auditiva ( Kayser y Logothetis, 2009 ). La codificaciÃģn temporal es por lo tanto utilizada junto con la codificaciÃģn espacial (es decir, quÃĐ poblaciones de neuronas estÃĄn activas) para maximizar la representaciÃģn de la informaciÃģn sensorial. Sabemos que hay diferentes frecuencias oscilatorias en el cerebro humano gracias a los estudios de EEG (electroencefalografÃa 1 1
La electroencefalografÃa (EEG) y la magnetoencefalografÃa (MEG) son dos tÃĐcnicas de registro electrofisiolÃģgico de la actividad elÃĐctrica cerebral en curso en diferentes frecuencias oscilatorias por medio de electrodos o sensores que se sitÚan en o sobre la totalidad de cuero cabelludo.
). Estos estudios muestran la existencia de actividad elÃĐctrica en diferentes bandas de frecuencia en el cerebro en reposo (p. ej., delta, 0.5-4 Hz, theta, 4-8 Hz, gamma, 30-80 Hz; vÃĐase Buzsaki, 200 6). MÃĄs recientemente, se ha despertado un gran interÃĐs respecto a si diferentes redes neuronales del cerebro oscilan preferentemente a determinadas frecuencias, lo que les facilitarÃa la codificaciÃģn de la informaciÃģn sensorial entrante mediante su âajuste de faseâ o acoplamiento a las mismas frecuencias que el input. El input auditivo contiene frecuencias temporales muy diversas y el input visual contiene frecuencias espaciales muy diversas.Durante la percepciÃģn del habla, los estudios de neurociencia cognitiva en adultos sugieren que el que aquella estÃĐ âajustada en faseâ (cuando la fase de una seÃąal oscilante se acopla a la fase o tiempo de una seÃąal [ input ] de referencia) en la frecuencia theta en el giro de Heschl determina el encadenamiento silÃĄbico del habla y su inteligibilidad subsiguiente ( Luo y Poeppel, 2007 ). El giro de Heschl se encuentra en el la corteza auditiva primaria, y la frecuencia theta es aproximadamente la frecuencia en la que se producen las sÃlabas en todas las lenguas del mundo (vÃĐase Poeppel et al., 2008 ). Se piensa que redes neurales en esta ÃĄrea de la corteza auditiva utilizan elementos de la seÃąal entrante tales como los tiempos de subida para reajustar su actividad oscilatoria, de manera que su frecuencia oscilatoria natural estÃĐ en fase con el input, lo que potencia el procesamiento sensorial (vÃĐase Goswami, 2011 ). En el modelo de resoluciÃģn multi-tiempo ( Hickok y Poeppel, 2007 ), las redes neurales que muestrean la entrada a frecuencias rÃĄpidas (gamma) y lentas (theta) se asumen como subyacentes a ventanas de integraciÃģn temporal para el habla rÃĄpidas vs. lentas. Por ejemplo, Luo y Poeppel (2007) demostraron usando la MEG (magnoencefalografÃa 1 ) que el patrÃģn de fase de las respuestas en banda theta (4-8 Hz) registradas en la corteza auditiva humana procesaban y discriminaban las oraciones habladas de forma fiable. El periodo de la oscilaciÃģn theta (una ventana temporal de unos 200 ms) parecÃa reajustarse a la informaciÃģn entrante del habla para procesar su dinÃĄmica, permitiendo la segmentaciÃģn de la seÃąal entrante en unidades del tamaÃąo de una sÃlaba que podrÃan ser utilizadas para acceder a las formas auditivas de las palabras del lÃĐxico mental. Luo y Poeppel defendieron, a la vista de sus datos, que la sÃlaba serÃa un primitivo computacional en el procesamiento cortical del habla, una sugerencia que es respaldada por los mÃĄs recientes trabajos tanto sobre mÃĄquinas de reconocimiento lingÞÃstico como por la propia lingÞÃstica ( Greenberg, 2006 ). A pesar de sus evidentes implicaciones para la pedagogÃa, esta perspectiva aÚn necesita asentarse en la educaciÃģn de la lectura asà como en los estudios conductuales sobre lectura.
ÂŋPermite el modelo neurocientÃfico predecir el comportamiento?Ahora utilizaremos este marco conceptual de la neurociencia de la audiciÃģn para hacer predicciones sobre el comportamiento de los niÃąos. Por ejemplo, a nivel cerebral podemos explorar si la percepciÃģn silÃĄbica y la inteligibilidad del habla estÃĄn relacionadas con el patrÃģn de fase de la banda theta, tanto en niÃąos como en bebÃĐs. Los bebÃĐs reconocen su propio nombre en torno a los 4 meses de edad y producen sus primeras palabras en torno a los 9 meses ( Bortfeld, Morgan, Golinkoff y Rathbun, 2005; Fenson et al., 1994 ). Dado que tanto la frecuencia oscilatoria theta como la gamma parecen intrÃnsecas a la corteza auditiva humana ( Giraud et al., 2008 ), los fenÃģmenos de reacoplamiento y sincronizaciÃģn de fase podrÃan estudiarse en el primer aÃąo de vida y relacionarse con el desarrollo lingÞÃstico y fonolÃģgico ( Telkemeyer et al., 2011 ). Dichas medidas tambiÃĐn podrÃan proporcionar marcadores neurales del riesgo de desÃģrdenes fonolÃģgicos tales como la dislexia ( Lyytinen et al., 2001 ), al igual que la sensibilidad al tiempo de subida medida en las primeras fases del desarrollo ( Goswami, 2009 ). TambiÃĐn podemos explorar si la eficacia del ajuste de fase en el giro de Heschl predice el desarrollo lingÞÃstico y fonolÃģgico de los niÃąos, asà como si el ajuste de fase a la envolvente de amplitud del habla es deficiente en la dislexia. De hecho, ya existe alguna evidencia a favor de esta Última predicciÃģn. Abrams, Nicol, Zecker y Kraus (2009) usaron EEG para medir el ajuste de fase al habla correlacionando la respuesta obtenida en electrodos situados sobre la corteza temporal (que contiene al giro de Heschl) con la envolvente general de frecuencias de una oraciÃģn repetida cientos de veces (âel chico joven abandonÃģ su casaâ). Se encontrÃģ que los malos lectores de 12 aÃąos mostraban un deficiente acoplamiento de fase a esta oraciÃģn. AdemÃĄs, se observaron diferencias interhemisfÃĐricas en el tiempo de ajuste de fase en funciÃģn de las habilidades lectoras. Los lectores de 12 aÃąos con un desarrollo tÃpico mostraban que el acoplamiento empezaba antes en el hemisferio derecho, lo que estarÃa de acuerdo con el modelo de Hickok y Poeppel (2007) . Por contra, en los malos lectores el acoplamiento comenzaba antes en su hemisferio izquierdo. Esta asimetrÃa cortical explicaba el 50% de la varianza en las habilidades lectoras de los niÃąos.
A nivel comportamental, podrÃamos esperar que los niÃąos con dislexia mostraran dificultades fonolÃģgicas relacionadas con aspectos suprasegmentales del habla, tales como dificultades prosÃģdicas y de acento silÃĄbico. Estas dificultades fonolÃģgicas aparecerÃan para todo tipo de tareas lingÞÃsticas mÃĐtricas (la estructura mÃĐtrica se refiere a la alternancia de âgolpesâ silÃĄbicos fuertes y dÃĐbiles en el lenguaje). De hecho, las dificultades pueden aparecer tambiÃĐn en otras tareas rÃtmicas que impliquen estructura mÃĐtrica, tales como tareas musicales o incluso tareas simples de percepciÃģn rÃtmica que tambiÃĐn requieran un ajuste o acoplamiento de fase apropiado al input rÃtmico por parte de la redes neurales auditivas. Un ejemplo serÃa el golpear en tiempo respecto a un ritmo. La investigaciÃģn mÃĄs reciente avala al menos algunas de estas predicciones.
La percepciÃģn prosÃģdica puede medirse mediante tareas de lenguaje reiterativas, en las que las sÃlabas fuertes se sustituyen por âDiâ y las dÃĐbiles por âdiâ (de manera que, p. ej., âcajÃģn azulâ se convierte en diDididi; Kitzen, 2001 ). Los niÃąos con dislexia a los que se les administra una tarea DiDi muestran un pobre reconocimiento de fotografÃas de famosos mencionadas en âDidisâ (Harry Potter como DidiDidi; vÃĐase Goswami et al., 2010 ). Las diferencias individuales en la sensibilidad a la estructura DiDi se podÃan predecir en funciÃģn de la capacidad de discriminaciÃģn de los tiempos de subida. La percepciÃģn del acento silÃĄbico tambiÃĐn se puede medir directamente. En un estudio se pidiÃģ a un grupo de dislÃĐxicos adultos que juzgaran si dos palabras de 4 sÃlabas se acentuaban de la misma manera (p. ej., âparÃĐntesisâ, âridÃculoâ; Leong, HÃĪmÃĪlÃĪlinen, Soltesz y Goswami, 2011 ). Los adultos con dislexia fueron significativamente menos sensibles a la acentuaciÃģn silÃĄbica y las diferencias individuales en dicha sensibilidad se podÃan predecir a partir de la discriminaciÃģn del tiempo de subida y no por otras medidas auditivas (discriminaciÃģn de la frecuencia o de la intensidad). En datos sin publicar, tambiÃĐn hemos encontrado que la imitaciÃģn de la entonaciÃģn silÃĄbica dÃĐbil-fuerte y fuerte-dÃĐbil se encuentra mermada en niÃąos con dislexia, que tambiÃĐn fueron peores a la hora de usar la acentuaciÃģn para diferenciar MAma (fuerte-dÃĐbil) de maMA (dÃĐbil-fuerte; Huss y Goswami, datos sin publicar).
Respecto a dÃĐficits rÃtmicos mÃĄs generales, mantener el ritmo de un metrÃģnomo golpeando con los dedos (acoplamiento rÃtmico) parece estar empobrecido para las tasas relevantes para las sÃlabas en la dislexia del desarrollo ( Thomson y Goswami, 2008; Thomson, Fryer, Maltby y Goswami, 2006 ). Se pidiÃģ a niÃąos y adultos con dislexia que golpearan sÃncronamente a ritmos a una tasa de 1.5 Hz (666 ms), 2 Hz (500 ms) y 2.5 Hz (400 ms). Mientras que todos los niÃąos mostraban dificultades a 1.5 Hz (666 ms), sÃģlo los niÃąos con dislexia tambiÃĐn mostraban dificultades a 2.5 Hz (400 ms) y a 2 Hz (500 ms). Los adultos con dislexia, por su parte, mostraban dificultades a 1.5 Hz y a 2 Hz en comparaciÃģn con lectores normales, pero no a 2.5 Hz. Las diferencias individuales en el acoplamiento rÃtmico se podÃan predecir a partir de la discriminaciÃģn del tiempo de subida, tanto en niÃąos como en adultos. En una tarea musical mÃĐtrica, en la que âmelodÃasâ cortas que contenÃan tres repeticiones de frases de 2-5 notas se presentaban a niÃąos con y sin dislexia en un paradigma de juicio semejante-diferente, se encontrÃģ una sensibilidad a la estructura mÃĐtrica significativamente menor en los niÃąos con dislexia ( Huss, Verney, Fosker, Fegan y Goswami, 2011 ). Aunque la complejidad mÃĐtrica se variaba ubicando la nota mÃĄs baja en la primera, segunda o tercera posiciÃģn y utilizando secuencias con notas de diferente longitud (aunque no de diferente longitud perceptiva general), los niÃąos con dislexia mostraban perores resultados a la hora de determinar si dos melodÃas eran la misma incluso para las secuencias mÃĄs fÃĄciles (p. ej., 2 notas alternando 3 veces, con un aumento de la duraciÃģn entre las notas en la segunda presentaciÃģn de la melodÃa). En el estudio de Huss et al. (2011) fue la discriminaciÃģn del tiempo de subida mÃĄs que de la duraciÃģn lo que predijo las diferencias individuales.
ÂŋQuÃĐ tÃĐcnicas de imagen cerebral son mÃĄs relevantes para su uso en pedagogÃa?Cualquier input ambiental, incluyendo los ambientes de aprendizaje ofrecidos en entornos educativos, afectarÃĄ a los procesos fisiolÃģgicos del cerebro. Respecto a la estructura conceptual desarrollada hasta ahora, parecerÃa del mayor interÃĐs poder comprender hasta quÃĐ punto las prÃĄcticas tradicionales utilizadas en las escuelas infantiles, tales como las canciones infantiles (que normalmente son poemas mÃĐtricos), o el uso de la poesÃa en las canciones y en el aprendizaje afectan a los procesos fisiolÃģgicos que parecen (segÚn los anÃĄlisis expuestos aquÃ) ser importantes para percibir las estructuras silÃĄbica y mÃĐtrica del lenguaje. SerÃa de mayor interÃĐs indagar si las practicas pedagÃģgicas basadas en juegos lingÞÃsticos (tales como juegos rÃtmicos, juegos de sÃlabas) o en la combinaciÃģn de movimientos motores con lenguaje (dar una palmada por cada sÃlaba, marchar al ritmo de sÃlabas) o en cantar con mÚsica (donde la estructura temporal de la mÚsica debe coordinarse con la estructura temporal del lenguaje mediante alineamiento estructural rÃtmico) modulan la actividad de las redes oscilatorias theta medidas por Luo y Poeppel (2007) . HipotÃĐticamente, estas actividades educativas deberÃan sincronizar las oscilaciones a frecuencias bajas en el giro de Heschl (theta y delta), que parecen ajustadas en fase a los patrones rÃtmicos silÃĄbicos y de entonaciÃģn del habla. La predicciÃģn serÃa que la eficacia en el ajuste de fase (es decir, acoplamiento) de estas oscilaciones theta mejorarÃa en los niÃąos mediante el juego lingÞÃstico. Si estas formas de juego lingÞÃstico realmente mejoran el ajuste de fase de theta en la corteza auditiva y si esta mejora estÃĄ vinculada con una conciencia fonolÃģgica mayor, entonces la neurociencia educacional habrÃĄ proporcionado una evidencia contundente de que esas pedagogÃas son importantes para una educaciÃģn eficiente de la alfabetizaciÃģn en los primeros aÃąos. Una aproximaciÃģn neurocientÃfica permitirÃa por tanto valorar directamente los mecanismos causales implicados en el desarrollo. La eficacia del ajuste de fase es la variable dependiente, el juego lingÞÃstico es la intervenciÃģn educativa y un cambio en la variable dependiente tras la intervenciÃģn sugerirÃa la existencia de una relaciÃģn positiva entre el juego lingÞÃstico y la eficacia del sustrato fisiolÃģgico para la codificaciÃģn lingÞÃstica. Como suele ocurrir en los estudios de desarrollo, habrÃa que eliminar terceras variables posibles y serÃa importante probar los efectos de la intervenciÃģn en diferentes ÃĄmbitos y poblaciones. La cuestiÃģn conceptual aquà es que una variable dependiente neural, como es la eficacia en el ajuste de fase, puede ser utilizada para comparar diferentes formas de intervenciÃģn educativa temprana que pretendan potenciar el lenguaje de los niÃąos y el desarrollo de la alfabetizaciÃģn e igualmente puede decirnos quÃĐ intervenciones presentan resultados tangibles sobre el sistema neural del niÃąo para el lenguaje (en lugar de, por ejemplo, sobre la confianza o la auto-estima del niÃąo âque tambiÃĐn serÃa importante desde el punto de vista educativo, pero que implicarÃa mecanismos de desarrollo diferentes).
AdemÃĄs, dichos estudios neurocientÃficos podrÃan constituir una razÃģn para proporcionar experiencias educativas rÃtmicas y musicales extra a los niÃąos que pueden correr el riesgo de padecer dificultades lectoras y por lo tanto para probar si realmente actÚan afectando al sistema lingÞÃstico en desarrollo. Dado que el cerebro es un sistema muy complejo e integrado, es posible que durante el desarrollo las experiencias tempranas que suplementan los ritmos auditivos con (pongamos por caso) ritmos motores (como por ejemplo al marchar al ritmo de la mÚsica) pueden o bien fortalecer los diferentes mecanismos de codificaciÃģn que serÃĄn la base del ajuste rÃtmico auditivo (p. ej., mediante estructuras subcorticales como el cerebelo) o bien ejercer un efecto directo sobre la eficacia de los mecanismos oscilatorios la misma corteza auditiva (p. ej., mediante la integraciÃģn multisensorial). Para la educaciÃģn, lo que realmente importa es que ÃĐstas son cuestiones empÃricas que pueden ser evaluadas y por lo tanto refutadas si son incorrectas. Son predicciones fisiolÃģgicas que estÃĄn abiertas a verificaciÃģn cientÃfica y falsaciÃģn. Si marchar al ritmo de la mÚsica ajusta las oscilaciones theta, este deberÃa ser el caso independientemente del contexto o situaciÃģn de aprendizaje (aunque tÃĐngase en cuenta que un Ãndice fisiolÃģgico del aprendizaje tambiÃĐn nos permitirÃa averiguar si algunos contextos de aprendizaje son realmente mÃĄs eficaces que otros para el acoplamiento âÂĄtales como aquellos que sean mÃĄs divertidos!).
TÃĐngase en cuenta igualmente que dichas medidas tambiÃĐn nos proporcionarÃan una herramienta para poder probar los efectos de otras intervenciones educativas, por ejemplo intervenciones que se suponga remedien la dislexia del desarrollo. Un Ãndice neural que se ha visto ligado al desarrollo fonolÃģgico, tal como (hipotÃĐticamente) la eficacia del ajuste de fase en theta, podrÃa emplearse para discriminar entre intervenciones educativas eficaces e ineficaces. Por ejemplo, cabrÃa esperar que las intervenciones ineficaces tambiÃĐn produzcan cambios en los procesos fisiolÃģgicos del cerebro, pero podrÃa ser que sus efectos tuvieran lugar en sistemas neurales muy diferentes, quizÃĄ sistemas que no tengan ninguna relaciÃģn con el lenguaje. Como los procesos fisiolÃģgicos son independientes de la atenciÃģn y un proceso fisiolÃģgico como el ajuste de fase de las oscilaciones neuronales no puede (por lo que sabemos) realizarse conscientemente para algunos estÃmulos pero sà para otros, el estudio sistemÃĄtico de aspectos muy bÃĄsicos de la codificaciÃģn de la informaciÃģn, tales como el ajuste de fase en diferentes sistemas neurales, tiene el potencial de proporcionar una base robusta para la educaciÃģn.
Un resultado interesante de los estudios con biofeedback es que los humanos adultos pueden ajustarse ivamente a frecuencias oscilatorias particulares en ÃĄreas concretas de la corteza para potenciar el aprendizaje motor. Rozengurt, Barnea y Reiner (2010) entrenaron a adultos a realizar una tarea de aprendizaje motor. A continuaciÃģn usaron neurofeedback del EEG en un ambiente virtual para aumentar o bien su potencia en la banda theta (que se espera consolide la memoria, pues la actividad theta estÃĄ relacionada con la consolidaciÃģn en memoria durante el sueÃąo) o bien la de la banda beta (una banda de frecuencia control). Un tercer grupo se tomÃģ un descanso en lugar de realizar el biofeedback . Mientras el grupo theta mostrÃģ una mejora significativa en el aprendizaje motor tanto al cabo de un dÃa, como de dos, como una semana mÃĄs tarde, que no fue el caso para el grupo de biofeedback beta ni para el grupo de control. Aunque el aprendizaje de secuencias de dedos no es una tarea que se enseÃąe en la escuela, estos estudios demostrarÃan en principio que incrementar la potencia del EEG en determinadas frecuencias puede mejorar el aprendizaje humano. Por lo tanto, si las canciones infantiles aumentan la potencia de la banda theta en la corteza auditiva, este serÃa un dato de relevancia para los educadores. QuizÃĄ merezca la pena resaltar que la neurociencia cognitiva basada en tales principios podrÃa suponer enormes beneficios educativos. Por ejemplo, en principio serÃa posible que surgieran nuevas intervenciones educativas formuladas con el objetivo de influir en determinadas frecuencias oscilatorias. Aquà he mostrado argumentos a favor de que algunas actividades tradicionalmente utilizadas en edades tempranas, tales como las canciones infantiles con juegos de rimas, la poesÃa, el canto y la mÚsica pueden afectar ivamente a la actividad oscilatoria theta en la corteza auditiva. No obstante, es posible que se consigan efectos similares con otras intervenciones no consideradas aquÃ, por ejemplo intervenciones basadas en los neurotransmisores que afectan especÃficamente a esta actividad oscilatoria. Todas las intervenciones tempranas tendrÃan un impacto importante sobre las subsiguientes trayectorias de desarrollo para la alfabetizaciÃģn. Por lo tanto, desde mi punto de vista, si este marco conceptual es aceptado, los estudios bÃĄsicos en neurociencia podrÃan tener un valor real para la educaciÃģn.
ConclusiÃģnEn esta discusiÃģn iva solo he pretendido ser muy ilustrativa, consciente de que mis propuestas son solo un posible marco de referencia para vincular la neurociencia cognitiva con la educaciÃģn (vÃĐase tambiÃĐn Goswami y Szucs, 2011; Nelson y Bloom, 1997 ). Espero haber podido mostrar el potencial que tiene la neurociencia cognitiva para realizar contribuciones Útiles para la educaciÃģn. Mi opiniÃģn es que para realizar una contribuciÃģn duradera a la educaciÃģn, la neurociencia educativa debe abordar en primer lugar cuestiones experimentales muy bÃĄsicas. Necesitamos saber cÃģmo se codifica y se transmite la informaciÃģn en el cerebro y cÃģmo se relacionan con el aprendizaje estos procesos fisiolÃģgicos. Un buen punto de partida serÃa el procesamiento sensorial y el aprendizaje sensorial (como reconociÃģ Piaget hace tiempo al poner el ÃĐnfasis en el aprendizaje sensorio-motor; Piaget, 1954 ). No obstante, los estudios experimentales sobre estos procesos bÃĄsicos deberÃan diseÃąarse considerando lo que ya sabemos sobre el desarrollo de los sistemas cognitivos relevantes para la educaciÃģn a partir de la investigaciÃģn en educaciÃģn y en psicologÃa. La investigaciÃģn bÃĄsica tambiÃĐn deberÃa tener en cuenta las teorÃas y los datos mÃĄs recientes de la neurociencia en general. Las teorÃas neurocientÃficas tambiÃĐn deberÃan ser relevantes para el desarrollo, aunque los trabajos sobre el desarrollo sean mÃĄs bien escasos dentro de la neurociencia (ÂĄlos bebÃĐs y los niÃąos no suelen ser tan fÃĄciles de tratar como los adultos o los animales!). En cualquier caso, la neurociencia como campo nos ofrece oportunidades Únicas para poder estudiar y comprender los mecanismos causales del desarrollo. Necesitamos explorar los procesos de desarrollo que construyen las redes neurales aparentemente especializadas del cerebro de los adultos, con el fin de influir en las trayectorias de desarrollo y los estados finales de estas redes. A medida que mejoremos nuestra comprensiÃģn de los mecanismos causales del desarrollo a nivel sensorial en todo el cerebro, podremos estudiar cÃģmo se relacionan entre sà esos mecanismos de aprendizaje y desarrollo para dar lugar a diferencias individuales en los logros educativos. Esto nos permitirÃa optimizar los ambientes educativos, tanto dentro como fuera de la escuela. TambiÃĐn nos permitirÃa responder a algunas cuestiones sobre la naturaleza del conocimiento y sobre cÃģmo aprendemos, asà como sobre quÃĐ constituye un ser humano y su buen hacer, cuestiones que son del mayor interÃĐs para la educaciÃģn.
Extended SummaryHere I set out one possible framework for linking basic research in neuroscience to pedagogical questions in education. I will endeavour to via the illustrative example of reading/dyslexia research that neuroscience has the âauthorityâ of making physiological discoveries that are open to empirical test and disconfirmation. I hope to that the use of these âreductionistâ methods has the potential to enrich considerably our understanding of children's learning and of how best to develop their potential.
Reading acquisition by children is predicted across languages by individual differences in children's awareness of the phonological (sound-based) structures of speech. This has been demonstrated in psychological and educational research by asking pre-reading and reading children to complete simple oral tasks such as counting the number of syllables in words or deciding whether words rhyme. âSuprasegmentalâ phonological awareness has also been shown to be important in explaining individual differences in reading. Suprasegmental awareness is awareness of the prosodic and stress patterns that characterise connected speech, when whole sentences or phrases rather than single words are the unit of phonological analysis. Indeed, as a lexicon of spoken word forms develops, both phonetic (âsegmentalâ) and prosodic (âsuprasegmentalâ) information is inextricably bound together in the phonological information stored by the brain for each word form. Across languages, the core perceptual unit reflecting these sound structures is now thought to be the syllable rather than the phoneme.
These different phonological and other skills are impaired in children who have developmental dyslexia. The best predictor across languages of who will have problems in acquiring the orthography of that language is phonological awareness. Children with dyslexia in languages as phonologically and orthographically diverse as English, Italian, and Chinese all have phonological difficulties.
The primary sense underlying speech perception is audition. Babies are hearing speech even while in the womb, although what they can hear best is the low frequency modulations in speech. Accordingly, babies seem born with some awareness of the characteristic rhythmic patterns of their native language. Once the baby is interacting with social partners, however, visual information from lip, jaw, and cheek cues supplements auditory information in important ways. These âspeechreadingâ skills are important for efficiency in processing oral language. As we open and close our jaws to produce syllables, there is low frequency dynamic visual information centred at around 4 Hz. In turn, the low frequency auditory information in speech yields syllabic structure, and peaks at around 4-6 Hz. Hence, auditory and visual physiological mechanisms are converging to increase processing efficiency for language. Over the past decade, we have conducted a number of studies that suggest that the primary auditory difficulties for children with reading or language problems involve amplitude envelope processing. The amplitude envelope of speech refers to the fluctuations in sound intensity that reach the eardrums when listening to spoken language (see fig. 1 ). As speech is produced, energy (amplitude) rises and falls as syllables are produced and the jaws open and close. The ear then detects the different frequency bands in speech contained in the amplitude envelope and uses both amplitude (sound intensity) and frequency information to encode the signal. As a syllable is produced, energy will increase as the mouth opens, peaking at the production of the vowel. The rise time to the vowel, namely the onset of the amplitude envelope associated with a particular syllable, is a critical event in the speech signal, facilitating the temporal segmentation of the signal into syllables. Our data that the difficulties in phonological processing found in both children with developmental dyslexia or specific language impairment (SLI) are strongly associated with inefficient basic auditory processing of rise time. Rise time perception in turn is crucial for developing the high-quality phonological representations of language d for the acquisition of literacy. Rise time discrimination is impaired in dyslexic children who speak English, French, Hungarian, Spanish, Chinese, and Finnish.
The brain processes speech over time, and it is a temporally complex signal. Many frequencies are varying at different time scales and at different intensities. According to the model by Hickok y Poeppel (2007) , the cortex processes speech simultaneously on multiple time scales, particularly at two key temporal rates, a âsuprasegmentalâ or syllabic rate (with a long temporal integration window of 150-300 ms) and a âsegmentalâ or âphonemicâ (speech sound) rate, with a short temporal integration window of around 20-50 ms. For humans and speech processing, it seems likely that neuroelectric oscillations in different frequency bands effectively segment the incoming speech signal into âpacketsâ of information at different grain sizes. Via neural phase-locking (rhythmic entrainment) to incoming frequencies, the brain can track speech dynamics and discriminate spoken sentences, enabling speech to be understood. From EEG (electroencephalography), oscillatory frequencies in the human brain of interest here are Delta, 0.5-4 Hz, Theta, 4-8 Hz, and Gamma, 30-80 Hz. During speech perception, studies with adults suggest that there is a âphase lockingâ at the Theta rate in Heschl's gyrus that determines the syllabic parsing of speech and its consequent intelligibility. Networks of neurons in this area of auditory cortex are thought to use events in the incoming signal such as rise times to reset their oscillatory activity, so that their natural oscillatory rate is in phase with the input, thereby enhancing sensory processing.
As both Theta and Gamma oscillatory rates appear to be intrinsic to human auditory cortex, phase resetting and phase locking phenomena could be studied in the first year of life and related to linguistic and phonological development. Such measures may also provide neural markers of risk for phonological disorders such as dyslexia, as may rise time sensitivity measured early in development. We can also explore whether the efficiency of phase locking in Heschl's gyrus predicts children's language and phonological development, and whether phase locking to the amplitude envelope of speech is impaired in dyslexia. Indeed, there is already some evidence supporting the latter prediction.
It would be extremely interesting to examine whether early pedagogical practices based on language play (rhyming games, syllable games) or on combining motor movements with language (clapping out syllable rhythms, marching in time to syllable beats), or singing to music (where the temporal structure of music must be co-ordinated with the temporal structure of language by aligning rhythmic structure) modulate the activity of the Theta oscillatory networks. By hypothesis, these educational activities should entrain the lower frequency oscillations in Heschl's gyrus (Theta and Delta), which appear to phase-lock to the syllable rate and to the intonational patterning of speech. The prediction is that the efficiency of phase locking (i.e., entrainment) of these Theta oscillators would be improved by children's language play. The conceptual point here is that a neural dependent variable, such as efficiency of phase locking, can be used to compare different forms of early educational intervention aimed at boosting children's language and literacy development, and can also tell us which interventions actually have their effects on the child's neural system for language. Further, such neuroscience studies could provide a rationale for giving children who may be at risk of reading difficulties extra rhythmic and musical educational experiences.
FinanciaciÃģnUsha Goswami fue financiada por una Major Research Fellowship del Leverhulme Trust y una ayuda del Medical Research Council (G0902375).
Conflicto de interesesLa autora de este artÃculo declara que no tiene ningÚn conflicto de intereses.
El artÃculo original fue publicado en inglÃĐs por la British Psychological Society (BPS); Friederikson, N. y Laurillard, D. (Eds.) (2012). Educational Neuroscience. BJEP Monograph Series II, 8 , 129-142. La BPS no se hace responsable de la exactitud de esta traducciÃģn.
Copyright © 2024. Colegio Oficial de la Psicología de Madrid








 CrossRef
CrossRef






